No reino do microbioma intestinal, Akkermansia muciniphila (abreviação de bactéria Akk) há muito é celebrada como um "probiótico estelar". No entanto, um estudo recente de uma equipe de pesquisa da Universidade de Tsinghua, publicado na Nature Microbiology, apresentou uma impressionante "inversão de papéis" para este chamado "guardião intestinal"-revelando que, em condições imunológicas específicas, a bactéria Akk aparentemente inofensiva pode se transformar em cúmplice de patógenos, secretamente exacerbando a escalada de infecções intestinais. Como esse drama de "agente duplo" se desenrola no mundo microbiano?

O nome Akkermansia muciniphila-ou "bactéria Akk" para abreviar-já sugere sua estratégia de sobrevivência única: este micróbio "amante da mucina" depende principalmente da mucina, o principal componente da camada de muco intestinal, como sua fonte de alimento. Longe de ser um disruptor intestinal, este "comedor de muco" atua como um zelador intestinal dedicado, desempenhando vários papéis essenciais na manutenção do bem-estar digestivo:
Ao quebrar a mucina, as bactérias Akk estimulam continuamente as células epiteliais intestinais a se repararem e secretam mais muco, reconstruindo ativamente e mantendo uma barreira mucosa intestinal ideal-uma camada protetora que protege o intestino de invasores prejudiciais.
Por meio da metabolização da mucina, ela produz subprodutos benéficos como o butirato, um ácido graxo de cadeia curta que serve como fonte direta de energia para as células intestinais. Esses metabólitos também ajudam a regular o metabolismo energético do corpo, ligando a saúde intestinal à eficiência metabólica geral.
As bactérias Akk se comunicam diretamente com as células do sistema imunológico, ajustando a intensidade das respostas inflamatórias. Essa interação garante um equilíbrio delicado no sistema imunológico local do intestino, evitando a inflamação excessiva e a negligência imunológica.
Ao reforçar a barreira física do muco, as bactérias Akk criam um escudo robusto que impede que toxinas e patógenos penetrem no revestimento intestinal e entrem na corrente sanguínea, aumentando a primeira linha de defesa do intestino.
Este papel multifuncional-nutrir a camada de muco, reparar o intestino, regular a imunidade, e apoiando o metabolismo-solidificou o status de longa data da bactéria Akk como um "probiótico estelar" e um símbolo icônico da saúde intestinal.
A história deu uma guinada dramática quando os pesquisadores observaram infecções intestinais incomumente graves em um modelo sem células imunológicas ILC3-um paradoxo que descobriu um lado escuro oculto da bactéria Akk.
Em um intestino saudável, as células do sistema imunológico ILC3 atuam como "guardas de patrulha intestinal", secretando continuamente a citocina IL-22. Esta molécula atua como um revestimento protetor para células epiteliais intestinais, desempenhando duas funções principais:
· A. Reforço da barreira física: Ao aumentar a fucosilação, ele cria uma superfície mucosa lisa que bloqueia diretamente a adesão de bactérias patogênicas ao revestimento intestinal.
· B. Controle Metabólico: Ele regula precisamente os níveis de galactosilação, limitando as fontes de carbono disponíveis para o crescimento excessivo de bactérias Akk-mantendo sua população sob controle.
Sem as células ILC3, este sistema bem ajustado entra em colapso, desencadeando uma cascata perigosa:
1. Proliferação descontrolada: a galactosilação em células intestinais aumenta, fornecendo às bactérias Akk um "buffet ilimitado" de nutrientes. Isso faz com que sua população exploda exponencialmente.
2. Produção de metabólitos tóxicos: as bactérias Akk crescidas começam a inundar o intestino com succinato, um ácido graxo de cadeia curta que se torna prejudicial em níveis elevados:
· A. Alteração do microambiente: reduz o pH intestinal, criando um ambiente ideal para patógenos como o Citrobacter rodentium colonizarem e se multiplicarem.
· B. Ativação de patógenos: o succinato muda diretamente os genes patogênicos, incluindo os fatores de virulência Tir (adesina) e Ler (regulador da ilha de patogenicidade). Isso aumenta a capacidade dos patogens de aderir às células intestinais e secretar toxinas.
Esta "boa intenção gUma reação em cadeia errada "transforma a bactéria Akk de um protetor intestinal em um cúmplice silencioso de patógenos, amplificando exponencialmente a gravidade e o risco da infecção.
Este estudo revela pela primeira vez o intrincado mecanismo que rege o equilíbrio dinâmico entre o sistema imunológico do hospedeiro e a microbiota intestinal-uma dança delicada que determina se as bactérias agem como aliadas ou adversárias.
Células imunes ILC3 → Secrete IL-22 citocina → Inibir a galactosilação de células intestinais → Restringir o crescimento excessivo de bactérias Akk → Preserve a estabilidade da camada mucosa
Deficiência de ILC3 → IL-22 insuficiente → Galactosilação descontrolada → Proliferação explosiva de bactérias Akk → Secreção excessiva de succinato → Virulência aprimorada do patógeno
Essa descoberta destrói a crença convencional de que "os probióticos são universalmente benéficos", provando que o papel de um micróbio depende inteiramente do contexto imunológico do hospedeiro. Como as espécies em um ecossistema, a dominância não regulada de uma única cepa bacteriana-mesmo uma "benéfica"-pode inclinar a balança, interrompendo a homeostase geral do intestino.
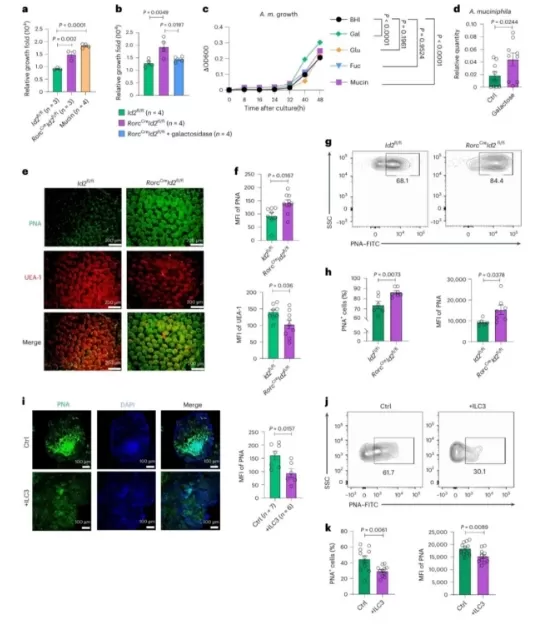
ILC3s regulam a glicosilação intestinal para restringir a proliferação de bactérias Akk
Esta pesquisa não diminui o potencial probiótico da bactéria Akk, mas serve como um lembrete crucial: o verdadeiro bem-estar intestinal está na compreensão da natureza dependente do contexto de nossos aliados microbianos. Aqui está o que significa para controlar a saúde intestinal:
Manter a função normal de células imunes como ILC3-which produzem a citocina protetora IL-22-may ser mais crítico do que simplesmente suplementar probióticos. Um sistema imunológico robusto atua como o "condutor" da microbiota intestinal, garantindo que bactérias benéficas como Akk permaneçam em seu papel protetor em vez de mudar para um estado prejudicial.
As bactérias intestinais não operam no vácuo-seus efeitos dependem do seu ambiente imunológico único. Avaliações de rotina de marcadores imunológicos (por exemplo, níveis de IL-22) juntamente com o perfil do microbioma podem ajudar a adaptar as intervenções: o que aumenta a saúde intestinal de uma pessoa pode sair pela culatra em alguém com disfunção imunológica.
A saúde intestinal é uma colaboração tripartida entre células imunológicas, células epiteliais intestinais e microbiota. Interrupções em qualquer componente-seja uma queda na atividade ILC3, uma barreira mucosa enfraquecida ou crescimento excessivo bacteriano não controlado-podem desencadear problemas em cascata. Nutrir esse ecossistema delicado requer uma abordagem holística, não apenas visando micróbios únicos.
À medida que repensamos o "probiótico de dupla natureza" que é a bactéria Akk, a lição é clara: a verdadeira saúde intestinal começa com o respeito à complexidade desse ecossistema interno. Em vez de perseguir soluções "tamanho único", priorizar a resiliência imunológica-a capacidade do próprio corpo de regular as interações microbianas-pode ser a chave para promover a coexistência harmoniosa entre nossas células e seus parceiros microbianos.
Como seu microbioma intestinal conversa com seu sistema imunológico?Siga o Campo Natural, um profissionalIngredientes de suporte imunológicoFabricante, para a mais recente pesquisa de saúde intestinal de ponta e junte-se a nós para desvendar os mistérios do microbioma humano!